
Los editoriales están elaborados por el equipo de Opinión de El Periódico y la dirección editorial

Editorial
Los editoriales están elaborados por el equipo de Opinión de El Periódico y la dirección editorial
Terapias avanzadas, seguras y a tiempo
Los tratamientos experimentales no deben quedar encallados ni arriesgar la seguridad del paciente
La UE estudia dejar a los hospitales sin poder desarrollar sus propias terapias avanzadas
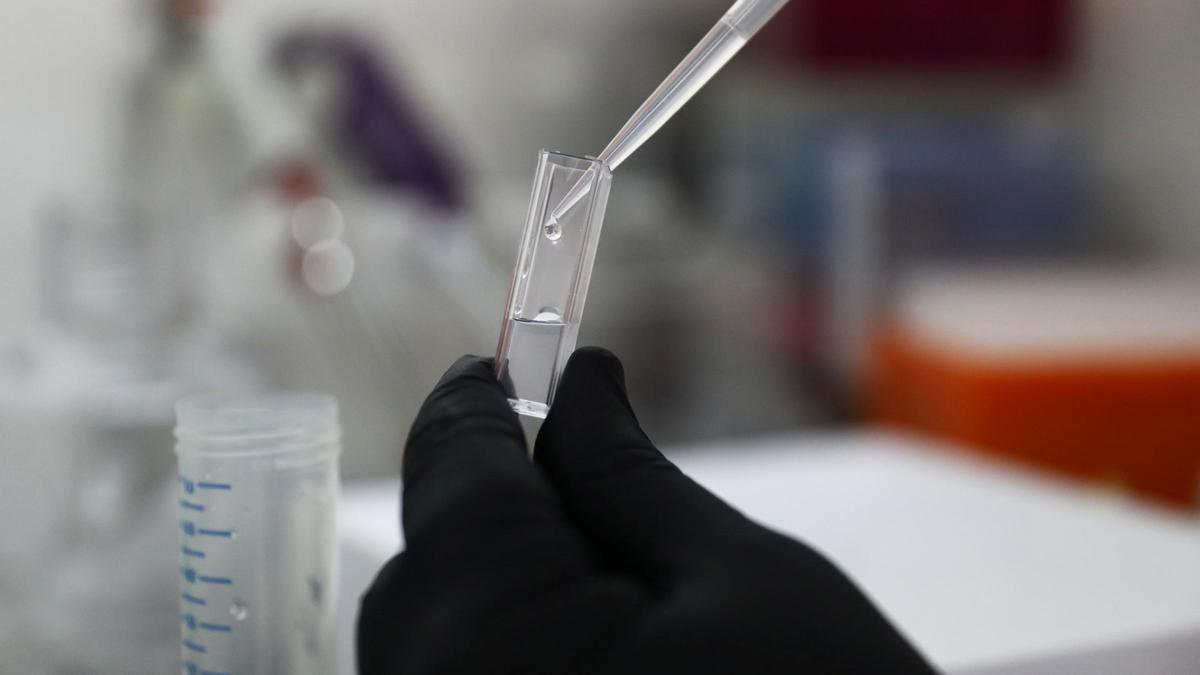
Ensayo clínico con un medicamento / EPC
Los avances de la investigación farmacológica movilizan miles de millones de euros de inversiones públicas y privadas. Mantienen un complejo sistema de investigación y desarrollo, público y privado, académico, clínico e industrial, que es especialmente relevante en entornos como Catalunya. Abren continuamente expectativas de curación o tratamiento de enfermedades hasta las que hace poco éramos impotentes. Y generan un gasto ingente para la sanidad pública. En todos y cada uno de estos aspectos se mantiene, o deben mantenerse, delicados equilibrios. La relación coste-beneficio debe justificar su financiación pública. Las necesidades de la salud comunitaria deben encontrarse con el interés de la industria, que no abordaría costosísimas inversiones sin expectativas de rentabilizarlas. La premura por tener a disposición soluciones terapéuticas prometedoras no debe soslayar las garantías necesarias para confirmar que las esperanzas depositadas en ensayos en laboratorio tienen eficacia terapéutica y para descartar posibles efectos secundarios que puedan ser, o no, asumibles.
Esta exigencia obliga a costosísimos, sucesivos y prolongados procesos de pruebas clínicas que incluso en casos de extrema emergencia, como fue la pandemia del covid-19, a lo sumo se pueden acelerar a un alto coste, pero no esquivar. Ante el coronavirus se logró una vacuna en tiempo récord, pero las cautelas también hicieron que se cayeran en el proceso alternativas ineficaces o inseguras.
En estos momento está en pleno debate en el Parlamento Europeo una nueva directiva sobre la estrategia farmacológica europea que aborda todos estos debates y que ha puesto en alerta a diversos colectivos, especialmente a centros de investigación ligados a grandes hospitales. En la UE está vigente desde 2007 una normativa sobre los medicamentos de terapia avanzada (MTA) que incluye la llamada «exención hospitalaria». Esta cláusula permite a centros punteros aplicar terapias aún experimentales a sus pacientes, incluyendo su producción a medida en sus propios laboratorios clínicos, obviando algunos de los pasos del sistema de autorización centralizado por la Agencia Europea del Medicamento que rige sobre la industria farmacéutica.
En estos momentos, los grupos parlamentarios popular y liberal en el Parlamento Europeo apoyan una enmienda, apadrinada por la industria, que acotaría la exención hospitalaria en términos que aún están por fijar. Según sus promotores, para reducir la incertidumbre sobre estos tratamientos aún experimentales y garantizar su uso seguro y responsable. Según quienes la critican, para favorecer los intereses comerciales puestos en cuestión por esta vía alternativa.
En esta polémica entran en juego intereses económicos (tanto de una parte como de otra) y sobre ella pesan también prejuicios sobre la actividad de un sector clave como el farmacéutico. Por encima de ellos, por lo que se debe velar es por mantener ese equilibrio necesario: que los beneficios lleguen a los pacientes que lo necesitan lo antes que sea posible sin ponerlos en riesgo. También cuando el número de beneficiarios quizá no anime a desarrollar comercialmente una terapia (o lleve a no desarrollarla tan rápido como los centros de investigación clínica podrían y los enfermos necesitarían). n
- Hacienda te devuelve 300 euros si tienes un hijo menor de 25 años y 900 si tienes dos: así tienes que ponerlo en la declaración de la renta
- Adiós a los cajones de la cocina: la solución con perchas que puedes colocar en cualquier parte
- El CEO publica la primera encuesta de la campaña de las elecciones en Catalunya
- Buenas noticias para los jubilados: la paga extra de verano viene con sorpresa
- Tiempo de Catalunya, hoy, viernes 26 de abril: empieza un esperanzador episodio de lluvias
- Precintan un local de Castelldefels por incumplir la normativa de seguridad, salubridad e higiene
- Pedro Sánchez, en directo hoy: las últimas noticias tras la carta del presidente sobre su posible dimisión y reacciones
- RTVE elimina el último programa de Masterchef en el que se denigró a una concursante que abandonó por estrés