La lucha contra la pandemia
La UE inicia el proceso para autorizar la vacuna de CureVac
La Agencia Europa del Medicamento empieza el análisis en tiempo real de los datos del inyectable de la farmacéutica alemana
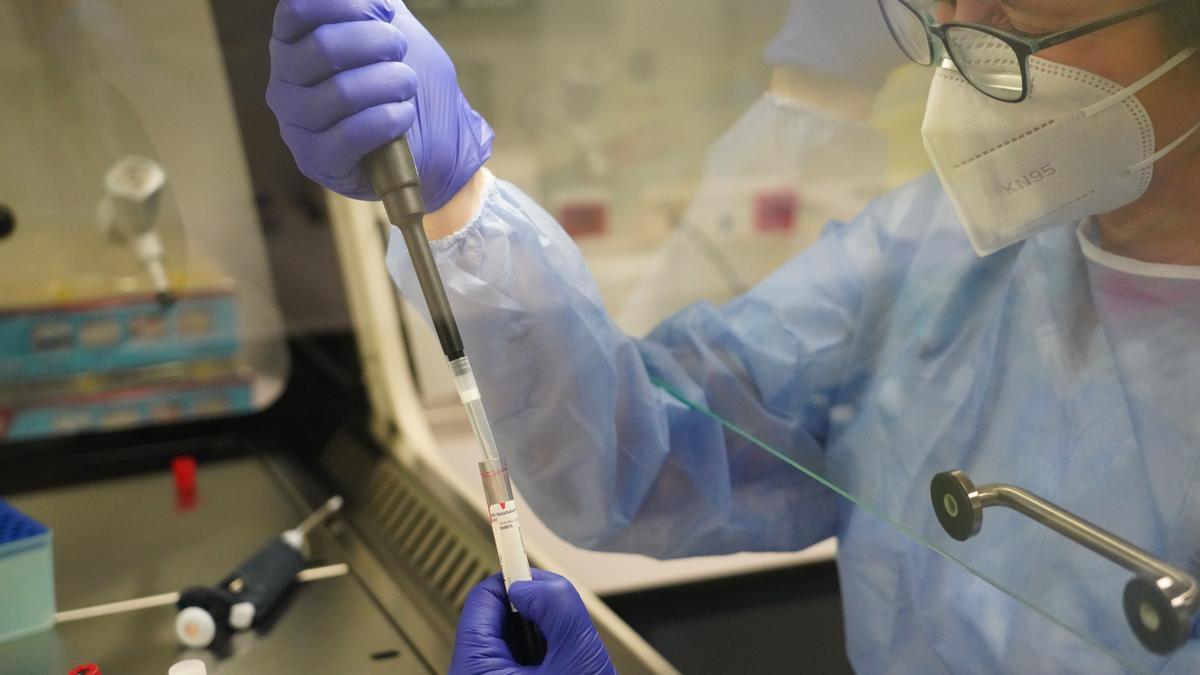
La Agencia Europea del Medicamento empieza a analizar en tiempo real los datos de la vacuna de CureVac. En la foto, una enfermera, durante el ensayo clínico de la vacuna alemana Curevac, en el Hospital de Cruces de Bilbao. /
La Unión Europea ha iniciado el proceso para la próxima autorización de la vacuna de CureVac contra el coronavirus. La Agencia Europea del Medicamento (EMA) ha empezado este viernes a analizar en tiempo real los datos de este inyectable desarrollado por el laboratorio alemán CureVac, un proceso que podría desembocar en una licencia de uso condicional de este fármaco en la UE. La EMA también tiene en fase de análisis la vacuna de Janssen (Johnson & Johnson).
Según el regulador europeo, la decisión de iniciar un proceso de “revisión continua” la tomó el comité de medicamentos humanos (CHMP) en base a los resultados preliminares de estudios de laboratorio y los primeros resultados clínicos de ensayos en adultos, que “sugieren que la vacuna desencadena la producción de anticuerpos” contra el SARS-CoV-2.
La vacuna de CureVac se suma a la de Janssen, desarrollada por la farmacéutica estadounidense Johnson & Johnson, las únicas dos vacunas que están en este momento en un proceso avanzado de análisis en tiempo real por parte de la EMA.
Si reciben la autorización, Curevac y Janssen se sumarán a las vacunas de Pfizer/BioNTech, Moderna y AstraZeneca. Estas tres ya se están suministrando a la población de los estados miembros de la UE.
Sin calendario fijado
CureVac está llevando a cabo ensayos clínicos en un mayor número de voluntarios para evaluar la seguridad, la inmunogenicidad --capacidad de desencadenar una respuesta contra el virus-- y la efectividad de este antídoto, conocido como CVnCoV y que se basa en la misma tecnología mRNA de Moderna y Pfizer/Biontech.
El proceso de revisión en tiempo real, que se usa en situaciones de emergencia sanitaria, continuará hasta que CureVac haya reunido y presentado las suficientes evidencias que respalden la seguridad, la eficacia y la calidad de su vacuna como para presentar una solicitud de autorización de comercialización en la UE, algo para lo que la EMA aún no tiene un calendario fijado debido a la falta de información suficiente para predecir fechas.
No obstante, haber iniciado ya un proceso de revisión continua permitirá evaluar una posible solicitud de licencia en un tiempo inferior al habitual en situaciones sanitarias normales, porque parte del trabajo de análisis se habrá ya realizado en tiempo real, lo que ya ocurrió con las otras tres vacunas autorizadas en la UE en diciembre y enero.
El pasado día 1, el gigante químico alemán Bayer anunció que cooperará con la empresa Curevac en la producción de su vacuna contra el coronavirus. El laboratorio que desarrolló este antídoto cuenta con que hasta finales de este año podrá elaborar unas 300 millones de dosis, y para 2022, se proyecta la producción de otros 600 millones.
- Hacienda te devuelve 300 euros si tienes un hijo menor de 25 años y 900 si tienes dos: así tienes que ponerlo en la declaración de la renta
- Adiós a los cajones de la cocina: la solución con perchas que puedes colocar en cualquier parte
- Tiempo de Catalunya, hoy, viernes 26 de abril: empieza un esperanzador episodio de lluvias
- El CEO publica la primera encuesta de la campaña de las elecciones en Catalunya
- Precintan un local de Castelldefels por incumplir la normativa de seguridad, salubridad e higiene
- Pedro Sánchez, en directo hoy: las últimas noticias tras la carta del presidente sobre su posible dimisión y reacciones
- ¿Cuánto dinero ganará Rosa Peral tras ganar la batalla a Netflix?
- Buenas noticias para los jubilados: la paga extra de verano viene con sorpresa
