En algunos casos
La EMA considera la hinchazón facial un efecto secundario de Pfizer
Una de cada cuatro personas vacunadas experimentan efectos secundarios leves, en especial dolor de cabeza y fatiga
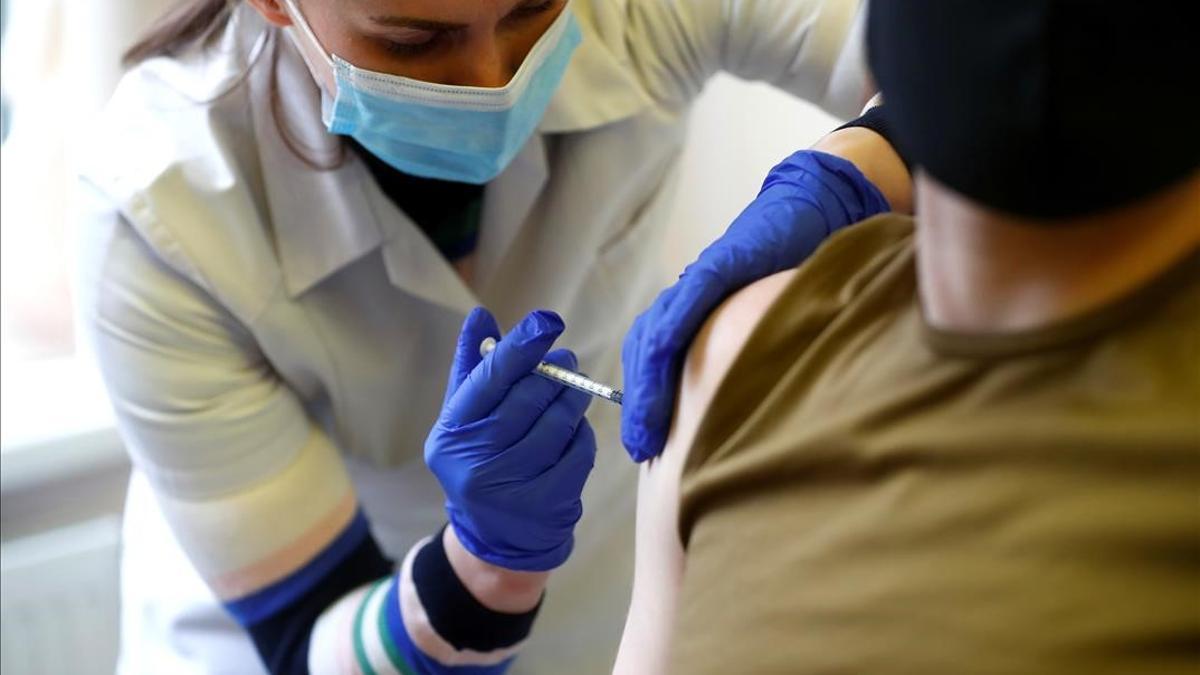
Latvian Army serviceman receives the Pfizer-BioNTech vaccine against the coronavirus disease (COVID-19) in Adazi Latvia May 7 2021 REUTERS Ints Kalnins / REUTERS / INTS KALNINS
La Agencia Europea del Medicamento (EMA) concluyó este viernes una investigación de varios casos de hinchazón facial tras la vacunación con Pfizer/BioNTech en personas con antecedentes de tratamientos de rellenos dérmicos y consideró que existe “al menos una posibilidad razonable” de que sea un efecto secundario de la vacuna.
Según las conclusiones alcanzadas por el comité de seguridad (PRAC), el hinchazón facial en personas con antecedentes de inyecciones con rellenos dérmicos debe incluirse en el prospecto como efecto secundario posible de la vacuna del covid-19 de Pfizer, aunque mantuvo que el balance entre beneficio y riesgo del fármaco sigue siendo positivo y “permanece sin cambios”.
Las campañas de vacunación masiva han sacado a la luz que varias personas vacunadas con Comirnaty, nombre comercial del preparado, desarrollaron esta reacción facial, según se refleja en todas las evidencias disponibles y los detalles que acompañan a los casos notificados en la base de datos europeos para presuntos efectos secundarios, EudraVigilance.
Este no era uno de los efectos adversos de Pfizer detectados durante los ensayos clínicos en voluntarios a los que se inyectó el preparado, lo que se hizo solo en un número determinado de personas.
Uno de cada cuatro vacunados, con efectos secundarios
“El PRAC consideró que existe al menos una posibilidad razonable de una asociación causal entre la vacuna y los casos notificados de hinchazón facial en personas con antecedentes de inyecciones con rellenos dérmicos, unas sustancias blandas similares a un gel que se inyectan debajo de la piel”, subraya la agencia. Este efecto secundario no se extiende al resto de la población que no cumple este perfil de antecedentes de rellenos dérmicos.
Una de cada cuatro personas vacunadas con Pfizer experimentan efectos secundarios sistémicos (no en el lugar del pinchazo) que son leves, en especial dolor de cabeza y fatiga, los cuales llegan a su punto álgido en las veinticuatro primeras horas y suelen durar entre uno y dos días, según un estudio realizado por el King's College de Londres.
Desde el inicio de las campañas de vacunación a finales del 2020, los efectos más frecuentes incluyeron escalofríos y temblores, diarrea, fiebre, artralgia (dolor de articulaciones), mialgia y náuseas, mientras que en el lugar de la inyección fueron dolor, hinchazón, sensibilidad, enrojecimiento, picor, calor e inflamación de las glándulas axilares.
Riesgo de pericarditis
La EMA también está “evaluando” casos de miocarditis y pericarditis notificados principalmente después de la vacunación con Pfizer, y analiza los casos de síndrome de Guillain-Barré (GBS) notificados tras inyecciones con AstraZeneca.
El regulador europeo explicó que “tiene conocimiento” de varios casos de miocarditis, inflamación del músculo cardiaco, y pericarditis, inflamación de la membrana alrededor del corazón, reportados por pacientes vacunados con Pfizer en los días posteriores a recibir la inyección, aunque “por el momento, no hay indicios de que estos casos se deban a la vacuna” de forma directa.
Sin embargo, el comité de seguridad (PRAC) de la EMA ha solicitado al laboratorio titular de la licencia de uso condicional en la Unión Europea (UE), BioNTech, que “proporcione datos más detallados, incluido un análisis de los eventos según la edad y el sexo”. Estos detalles serán analizados por el PRAC y compartidos en el próximo informe de seguridad de la pandemia, en el que también considerará si se necesita alguna otra medida reglamentaria relacionada con el uso de esta vacuna en la UE.
Además, el comité también ha solicitado a Moderna, que al igual que Pfizer usa una tecnología de ARN mensajero, que “controle casos similares con su vacuna y también proporcione un análisis detallado de los eventos” que puedan estar relacionados con miocarditis y pericarditis desarrollada en los días posteriores a la vacunación.
Por otro lado, y en relación con la vacunación con el preparado de AstraZeneca (Vaxzervia), la EMA también ha recibido informes sobre casos de síndrome de Guillain-Barré (GBS, por sus siglas en inglés), un trastorno poco común del sistema inmunológico que causa inflamación de los nervios y puede provocar dolor, entumecimiento, debilidad muscular y dificultad para caminar.
- Muere Itxaso Mardones, reportera de Gloria Serra en 'Equipo de investigación', a los 45 años
- Hacienda te devuelve 300 euros si tienes un hijo menor de 25 años y 900 si tienes dos: así tienes que ponerlo en la declaración de la renta
- ¿Llamadas que cuelgan? Así son las robollamadas, la nueva táctica de spam telefónico
- Adiós a los cajones de la cocina: la solución con perchas que puedes colocar en cualquier parte
- Sánchez se plantea renunciar y convocar elecciones tras la investigación a su esposa
- La querella del novio de Ayuso se admitirá a trámite pese a la campaña del fiscal para que sea rechazada
- El CIS publica una encuesta sobre las elecciones en Catalunya a pocas horas del comienzo de la campaña
- Pedro Sánchez se plantea renunciar como presidente del Gobierno tras la investigación a su mujer