Nuevo informe
La EMA vincula la vacuna de AstraZeneca con los casos raros de trombos
La Agencia Europea del Medicamento asegura que los beneficios de la vacuna superan a los riesgos y vuelve a respaldar su utilización
La Comisión Europea urge a los ministros de sanidad de la UE a seguir un enfoque coordinado para mejorar la confianza de los ciudadanos


Silvia Martinez
Periodista
La Agencia Europea del Medicamento (EMA) ha reconocido que existe “un posible vínculo” entre las personas vacunadas con el antídoto de AstraZeneca y los casos muy raros de coágulos sanguíneos inusuales notificados. Sin embargo, considera que los beneficios generales que aporta esta vacuna en la prevención del covid19 siguen superando a los riesgos de los posibles efectos secundarios.
“El comité de seguridad de la EMA ha concluido que los coágulos de sangre inusuales con plaquetas bajas en sangre deben incluirse como efectos secundarios muy raros de Vaxzevria (como se ha rebautizado a la vacuna de AstraZeneca)”, ha confirmado el comité de evaluación de riesgos y farmacovigilancia (PRAC) tras una última investigación en la que apunta que una explicación plausible para la combinación de coágulos sanguíneos y plaquetas bajas en sangre “es una respuesta inmune que conduce a una condición similar a la que se observa a veces en pacientes tratados con heparina”.
Por ello, la EMA ha vuelto a recomendar a los profesionales sanitarios y a todas las personas que reciban la vacuna de AstraZeneca que sean conscientes de la posibilidad de trombos durante las dos semanas posteriores a la inyección, conozcan los posibles síntomas y busquen atención médica urgente si sufren alguno de ellos (falta de aire, dolor en el pecho, dolor abdominal persistente, dolor de cabeza o visión borrosa entre otros).
Mujeres de menos de 60
Hasta ahora, según ha explicado la directora ejecutiva, Emer Cooke, la mayoría de los casos de coágulos sanguíneos se han producido en mujeres de menos de 60 años aunque con las evidencias actualmente disponibles “no se han confirmado factores de riesgo específicos” ni debido al género, la edad o las condiciones médicas previas.
"Aunque la mayoría de los casos han ocurrido en personas de menos de 60 años y en mujeres, por las diferentes formas en que se utiliza la vacuna en diferentes países, el PRAC no ha llegado a la conclusión de que la edad y el sexo sean factores de riesgo claros para estos efectos secundarios tan raros", ha indicado su responsable, Sabine Strauss.
Uso sin restricciones
Por ello, la EMA sigue sin recomendar limitar o restringir el uso de la vacuna e insiste en que debe seguir utilizándose. “El covid19 es una enfermedad muy grave con niveles de hospitalización y muertes muy elevados. La vacuna ha probado ser altamente efectiva para salvar vidas", ha asegurado Cooke, que considera "muy importante" utilizar las vacunas disponibles porque "el riesgo de mortalidad del covid19 es muy superior al riesgo de los efectos secundarios muy raros”.
El PRAC ha analizado en las últimas semanas un total de 62 casos de trombosis venosa cerebral (CVST) y 24 de trombosis esplénica venosa, notificados hasta el 22 de marzo, de los cuáles 18 fueron mortales. Hasta el 4 de abril, no obstante, los casos notificados al sistema EudraVigilancia suman 169 y 53 respectivamente en una población de 34 millones de personas vacunadas en el Espacio Económico Europeo y el Reino Unido.
Desde que obtuviera el visto bueno de la EMA para su comercialización el pasado 29 de enero, la vacuna de la farmacéutica AstraZeneca, la tercera autorizada en la UE, ha vivido en una montaña rusa. En primer lugar por la polémica entorno al contrato firmado por la UE con la empresa en nombre de los Veintisiete o los continuos problemas de producción del laboratorio y, en segundo, por el goteo de Estados miembros que decidieron paralizar la vacunación con este antídoto o limitarlo a algunos grupos de edad a raíz de los casos de trombos raros identificados.
Reunión de los Veintisiete
Convocados por la presidencia portuguesa de turno de la UE, los ministros de sanidad de los Veintisiete han abordado este miércoles las conclusiones del último dictamen de la EMA en un nuevo intento de aunar posiciones y tratar de armonizar los diferentes enfoques aplicados a la hora de administrar el antídoto de AstraZeneca. "La experiencia de AstraZeneca muestra que nuestro sistema de farmacovigilancia funciona. Pero es esencial que sigamos un enfoque coordinado en toda la Unión Europea: debemos hablar con una sola voz para aumentar la confianza del público en las vacunas", ha reclamado la comisaria de sanidad, Stella Kyriakides, que junto con la presidencia portuguesa de la UE ha apelado a todos los Estados miembros ha apelado a trabajar hacia "una posición lo más coordinada posible".
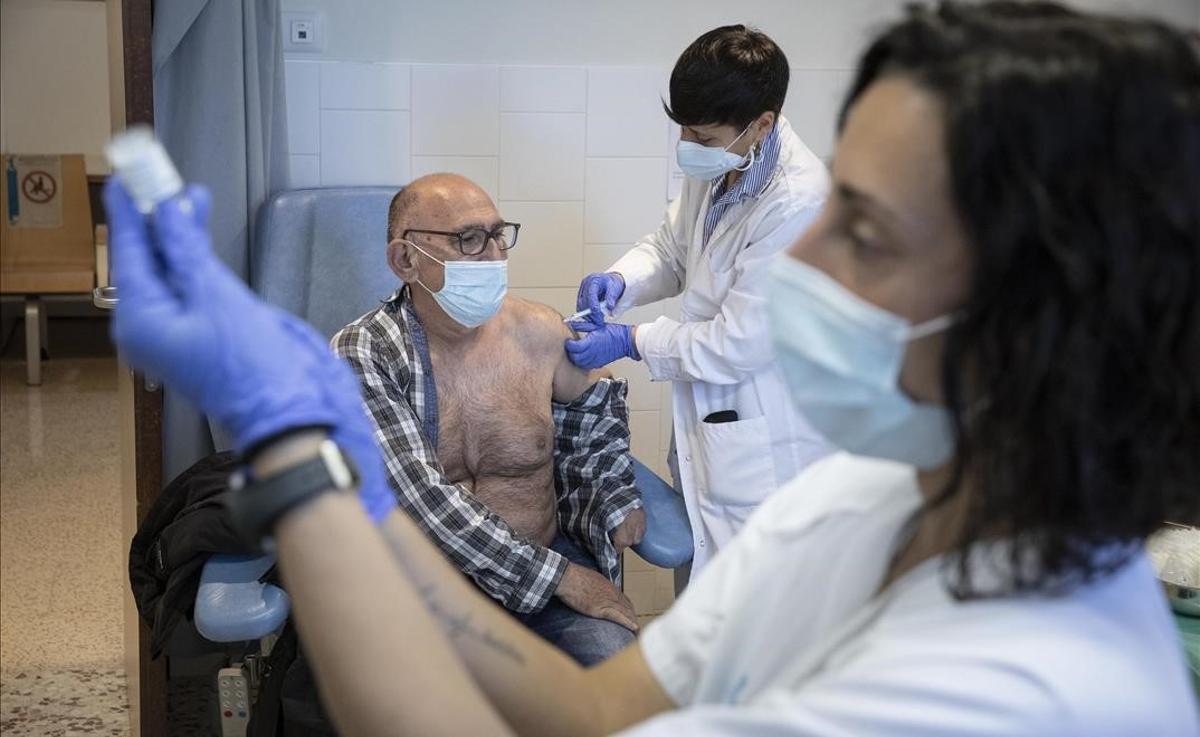
Barcelona 24 03 2021 Empiezan a vacunar de nuevo contra el covid con la vacuna de AstraZeneca en el CAP Casernes Foto de Ferran Nadeu / Ferran Nadeu
"Es una decisión técnica, no política. Debemos continuar siguiendo la mejor información científica aportada por la EMA. No hay que olvidar que las decisiones individuales afectan a todos", ha recordado la ministra de sanidad de Portugal, Marta Temido, en un comunicado en el que subrayan que los Ventisiete están de acuerdo en la necesidad de "más estudios de farmacovigilancia" sobre el impacto de las vacunas en los grupos específicos.
Países como Dinamarca o Noruega han optado por un enfoque de máxima prudencia y mantienen suspendida temporalmente la administración de la vacuna. Otros como Suecia decidieron el pasado 25 de marzo retomar las vacunaciones pero solo a los mayores de 65 años, lo mismo que Finlandia, mientras que Alemania solo la inyecta la personas de más de 60 años y Francia a mayores de 55 años. Tras la decisión de la EMA, Bélgica ha decidido este miércoles reservar este antídoto al menos durante las próximas cuatro semanas solo a los mayores de 55 años.
- García-Castellón y Gadea dejarán sus plazas en la Audiencia Nacional y Pedraz sopesa hacerse con el juzgado del Tsunami, por Ernesto Ekaizer
- El río subterráneo más largo de Europa está en España: nadie conoce su nacimiento ni su desembocadura
- Airbnb aconseja a los propietarios que no anuncien las piscinas en sus alojamientos turísticos
- Vuelve Moisés a Pasapalabra: el concursante desvela los problemas que sufrió en el pasado y por los que tuvo que abandonar el programa
- La Junta Electoral avala la candidatura de Puigdemont y rechaza la impugnación de Cs
- El invierno vuelve por Sant Jordi: los meteorólogos alertan del fenómeno que nos espera la próxima semana en Catalunya
- La vida de Rosa Peral en prisión: ¿A cuántos años está condenada? ¿Cómo es su día a día? ¿Qué estrategia seguirá en adelante?
- El Barça vive una tragedia insoportable ante el PSG