TERAPIA GÉNICA
Una terapia experimental cura la sordera congénita en ratones
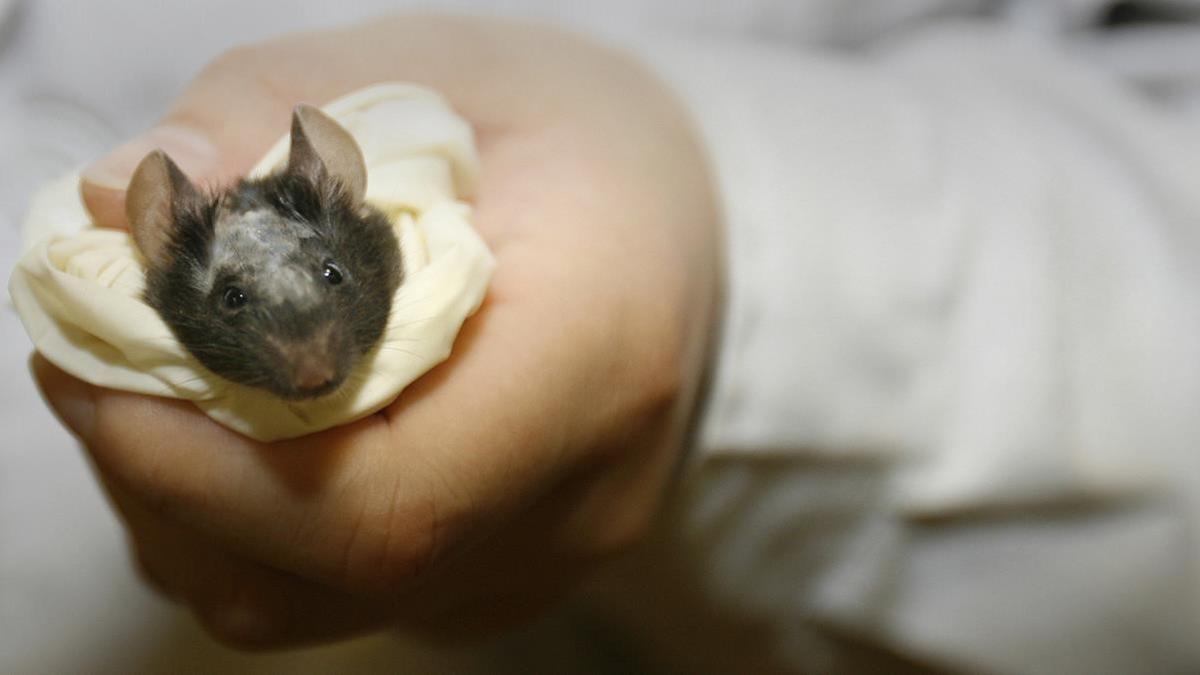
Uno de los ratones Beethoven sometidos a la terapia experimental contra la sordera congénita, en el Instituto Nacional de Ciencias Biológicas de Pekín. / periodico

Michele Catanzaro
Periodista
Michele Catanzaro
Un centenar de ratones Beethoven -así llamados porque sufren sordera congénita como el famoso músico- han vuelto a sobrecogerse ante fuertes ruidos, que antes ni tan solo notaban. Este comportamiento, que sugiere una recuperación del oído, se dio tras la aplicación de una terapia génica, cuyo resultado ha publicado en la revista 'Nature' el equipo de David Liu, investigador del Broad Institute (MIT y Universidad de Harvard, EEUU).
El sistema emplea la CRISPR, una técnica que desde el 2012 está revolucionando la biología, porque permite cortar genes 'erróneos' y pegar los 'correctos' (o incluso modificar letras individuales del ADN), con gran precisión y a muy bajo precio.
La sordera congénita se une así a la veintena de enfermedades (desde la retinosis pigmentaria hasta la distrofia muscular de Duchenne) que desde entonces se han tratado con la CRISPR en ratones y otros animales. Sin embargo, el salto a la terapia humana depende de muchos factores: entre ellos, su eficacia en los genes correspondientes en humanos, la capacidad de alterar un número suficiente de células para revertir la enfermedad y la seguridad de no modificar genes que no tocan.
"Es un trabajo fantástico: el primero que demuestra la eficacia de la CRISPR en la sordera", comenta Berta Alsina, investigadora experta en esta enfermedad de la Universitat Pompeu Fabra (UPF), no implicada en el trabajo.
Aproximadamente la mitad de los casos de sordera son congénitos. El problema se genera dentro del hueso temporal, en el oído interno. Allí, unas células en forma de pelo reaccionan vibrando a las ondas acústicas. Estas vibraciones modifican las propiedades de unas proteínas emplazadas en la base de cada 'pelo'. Esta modificación traduce la señal mecánica de la vibración en una señal eléctrica, que se transmite al cerebro y es lo que percibimos como sonido.
Unas proteínas, llamadas TMC1, están implicadas en este proceso en humanos. Si los genes que las producen tienen una alteración, las personas que nacen con esas mutaciones pueden quedar sordas. En concreto, si la mutación se da en los dos cromosomas que contienen este gen, la sordera se da desde el nacimiento. Si está solo en uno, se produce progresivamente a partir de la infancia. La diferencia entre el gen defectuoso y el que funciona correctamente es de tan solo una letra.
Las opciones de tratamiento son limitadas. "Hasta ahora, los intentos de terapia génica no habían prosperado en animales. Se había intentado con la introducción de células madre con los genes funcionantes, pero este proceso puede desencadenar un cáncer. También se había introducido directamente el gen funcionante, intentando que se sobreexpresara, pero tampoco había dado frutos", explica Alsina
El nuevo sistema, al contrario, explota la capacidad de la CRISPR de reemplazar el gen defectuoso por uno correcto. Los investigadores han introducido la maquinaria de 'corta y pega' del CRISPR en gotas de lípidos. Luego, han inyectado esta solución en el hueso temporal de un centenar de ratones Beethoven. Estos son ratones modificados para que tengan en las células de su oído interno la mutación genética que produce la sordera progresiva. Se llaman ratones Beethoven porque en ellos la sordera surge progresivamente, tal y como le ocurrió al músico.
Cuando la CRISPR alcanza las células, consigue corregir el gen defectuoso de algunas de ellas. "La gracia de la CRISPR es que es muy específica: identifica el gen mutado y modifica solo ese, sin afectar al gen sano presente en la misma célula", explica Alsina. Tampoco parecen producirse muchas modificaciones 'off-target': es decir, el mecanismo no modifica por error genes distintos al gen-objetivo.
El efecto sobre el animal es espectacular. Mientras el oído interno de un ratón Beethoven normal es casi del todo carente de las células ciliadas que captan el sonido vibrando, el de los ratones tratados con la CRISPR es casi indistinguible del de un ratón normal. Los primeros no reaccionan ante un sonido fuerte e imprevisto, mientras que los segundos saltan asustados. "La recuperación de la escucha varía de animal a animal, pero casi todos los animales recuperaron al menos un poco del oído", explica Liu.
No obstante, hay importantes limitaciones en el momento de imaginar una aplicación en humanos. "Al cabo de un mes, la efectividad del tratamiento se va reduciendo en ratones", observa Alsina. "La modificación se produce tan solo en una cierta porción de las células", añade Lluís Montoliu, investigador del Centro Nacional de Biotecnología (CNB), en Madrid, y uno de los referentes de la CRISPR en España.
Aunque los resultados sean prometedores, se deberán abordar estas cuestiones, antes de proceder con ensayos en humanos. Además, habrá que comprobar si el efecto es idéntico en el gen TMC1 humano. Finalmente, aunque el sistema produce pocas modificaciones genéticas indeseadas, en el caso humano es imprescibdible que incluso estas pocas no induzcan ningún efecto colateral.
Liu, posible candidato al Nobel
<span style="color: rgb(34, 34, 34); font-family: calibri; font-size: 16px; text-align: justify; background-color: rgb(255, 255, 255);">El autor del trabajo, David Liu, es uno de los pioneros de la CRISPR. Hace unos meses, Liu contribuyó a desarrollar su version más avanzada, que es capaz de editar letras de ADN una a una. Muchos científicos creen que es probable que en los próximos años los inventores de la CRISPR reciban un premio Nobel. No obstante, "el sistema de CRIPR empleado en este caso no es el más avanzado. Lo especial del estudio es la manera en que se lleva la CRISPR a las células", explica Lluís Montoliu, del CNB. Normalmente, los sistemas de edición genética se acoplan con unos virus, que penetran en las células de los animales vivos. Sin embargo, este sistema tiene el inconveniente de que el organismo puede generar una respuesta inmune. Además, las células del oído interno serían difíciles de alcanzar con este método, ya que están protegidas en el interior del hueso de la cóclea. "La idea de inyectar una solución lipídica es prometedora", afirma el investigador. Berta Alsina (UPF) coincide en ello, y destaca que este método ya se usa con otros objetivos en la clínica, lo que sienta un precedente para la futura aplicación del sistema en humanos.</span>
- Muere Itxaso Mardones, reportera de Gloria Serra en 'Equipo de investigación', a los 45 años
- Hacienda te devuelve 300 euros si tienes un hijo menor de 25 años y 900 si tienes dos: así tienes que ponerlo en la declaración de la renta
- ¿Llamadas que cuelgan? Así son las robollamadas, la nueva táctica de spam telefónico
- Adiós a los cajones de la cocina: la solución con perchas que puedes colocar en cualquier parte
- Sánchez se plantea renunciar y convocar elecciones tras la investigación a su esposa
- La querella del novio de Ayuso se admitirá a trámite pese a la campaña del fiscal para que sea rechazada
- El CIS publica una encuesta sobre las elecciones en Catalunya a pocas horas del comienzo de la campaña
- Pedro Sánchez se plantea renunciar como presidente del Gobierno tras la investigación a su mujer